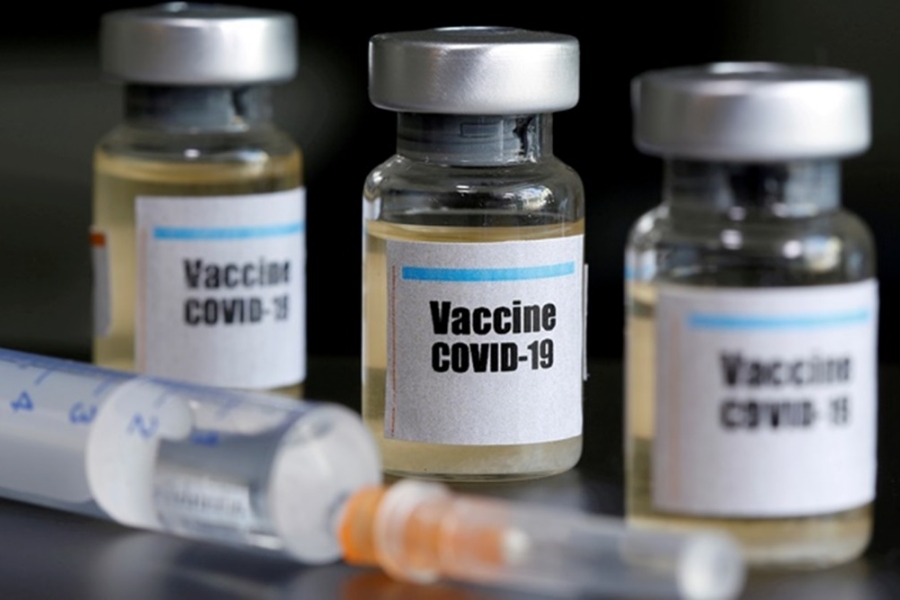
Την προκαταρκτική συμφωνία τους με την Ε.Ε. για 200 εκατ. δόσεις εμβολίου για την covid-19 ανακοίνωσαν η αμερικανική εταιρεία Pfizer και η γερμανική BioNTech. Εφόσον εγκριθεί το εμβόλιο, οι πρώτες δόσεις θα αρχίσουν να παραδίνονται έως το τέλος του 2020.
Οι εταιρείες ολοκλήρωσαν τις διερευνητικές συνομιλίες και εισέρχονται στις συμβατικές διαπραγματεύσεις με την Ευρωπαϊκή Επιτροπή για τη συγκεκριμένη προμήθεια. Επιδίωξη τους είναι η να εξασφαλιστεί και η δυνατότητα αγοράς επιπλέον 100 εκατ. δόσεων.
Το αίτημα αξιολόγησης του εμβολίου BNT162b2 από τις κανονιστικές αρχές θα κατατεθεί σύντομα, ενδεχομένως και τον προσεχή μήνα. Εφόσον εγκριθεί, θα παραχθεί στις μονάδες παραγωγής της BioNTech στη Γερμανία και στη μονάδα παραγωγής της Pfizer στο Βέλγιο.
1,3 δισ. δόσεις
Μετά την έγκριση από τις κανονιστικές αρχές, οι εν λόγω εταιρείες προγραμματίζουν με τα υπάρχοντα δεδομένα «να διαθέσουν έως και 100 εκατομμύρια δόσεις παγκοσμίως έως τα τέλη του 2020 και περίπου 1,3 δισεκατομμύρια δόσεις έως τα τέλη του 2021» σύμφωνα με την σχετική ανακοίνωση.
Εκτιμάται ότι η συμφωνία προμήθειας με την Ευρωπαϊκή Επιτροπή θα αποτελέσει τη μεγαλύτερη αρχική παραγγελία δόσεων εμβολίου στην ιστορία της Pfizer και της BioNTech έως τώρα.
«Η αναμενόμενη συμφωνία της Pfizer και της BioNTech με την Ευρωπαϊκή Επιτροπή αποτελεί ένα σημαντικό βήμα προόδου προς τον κοινό στόχο μας, που δεν είναι άλλος από το να μπορούμε να διαθέσουμε εκατομμύρια δόσεις του εμβολίου κατά της νόσου COVID-19 στους ευπαθείς πληθυσμούς πριν από το τέλος του έτους.», δήλωσε ο Albert Bourla, Πρόεδρος και Διευθύνων Σύμβουλος της Pfizer.
Οι προετοιμασίες έχουν αρχίσει καθώς ο ίδιος πρόσθεσε αναμένοντας την έγκριση από τις αρχές ότι «έχουμε ενεργοποιήσει την αλυσίδα εφοδιασμού μας, κυρίως τη μονάδα μας στο Βέλγιο, και έχουμε αρχίσει ήδη τις διαδικασίες παραγωγής».
Από την πλευρά του ο συνιδρυτής και Διευθύνων Σύμβουλος της BioNTech, Ugur Sahin, επεσήμανε ότι «στόχος μας είναι να αναπτύξουμε ένα ασφαλές και αποτελεσματικό εμβόλιο, που θα συμβάλει στην εξάλειψη αυτής της πανδημίας στην Ευρώπη και σε ολόκληρο τον κόσμο».
Το BNT162
Πρόκειται για εμβόλιο που βασίζεται στην ιδιόκτητη τεχνολογία mRNA της BioNTech και υποστηρίζεται από το παγκόσμιο πρόγραμμα ανάπτυξης εμβολίων και τις παρασκευαστικές ικανότητες της Pfizer.
Δύο από τα τέσσερα ερευνητικά υποψήφια εμβόλια των εταιρειών – BNT162b1 και BNT162b2 – έλαβαν πρόσφατα το χαρακτηρισμό «Fast Track» (διαδικασία ταχείας έγκρισης) από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ (FDA). Ο χαρακτηρισμός βασίστηκε στα προκαταρκτικά δεδομένα μελετών φάσης 1/2 στις Ηνωμένες Πολιτείες και τη Γερμανία, καθώς και από τις μελέτες ανοσογονικότητας σε ζώα.
«Κατά τη διάρκεια των προκλινικών και κλινικών μελετών, το BNT162b1 και το BNT162b2 αποδείχθηκαν ισχυροί υποψήφιοι, βάσει της αξιολόγησης της ασφάλειας και της ανοσολογικής απόκρισης» τονίζεται στην ανακοίνωση.
Μετά από αξιολόγηση των προκλινικών και κλινικών δεδομένων από τις κλινικές μελέτες φάσης 1/2, και σε συνεργασία με το Κέντρο Αξιολόγησης και Έρευνας Βιολογικών Παραγόντων (CBER) του FDA και άλλων κανονιστικών φορέων ανά τον κόσμο, επιλέχθηκε το υποψήφιο εμβόλιο BNT162b2 να προχωρήσει στη μελέτη φάσης 2/3. Συγκεκριμένα, το BNT162b2 κωδικοποιεί μια βελτιστοποιημένη, πλήρους μήκους γλυκοπρωτεΐνη της ακίδας του SARS–CoV-2 (S), η οποία αποτελεί τον στόχο των εξουδετερωτικών αντισωμάτων κατά του ιού.
Μελέτη φάσης 2/3
Στη μελέτη τελικού σταδίου εξετάζεται ένα δοσολογικό σχήμα 2 δόσεων σε επίπεδο δόσης 30µg σε έως και 30.000 συμμετέχοντες ηλικίας 18 έως 85 ετών, σε περίπου 120 κέντρα παγκοσμίως, συμπεριλαμβανομένων των περιοχών με σημαντική αναμενόμενη μετάδοση του SARS-CoV-2. Προσπάθεια γίνεται να συμπεριληφθεί ετερογενής πληθυσμός και εθελοντές, που διατρέχουν υψηλό κίνδυνο μόλυνσης από τον ιό. Έως σήμερα, έχουν εγγραφεί περισσότεροι από 25.000 συμμετέχοντες που λαμβάνουν ήδη τη 2η δόση.



















Comments (0)