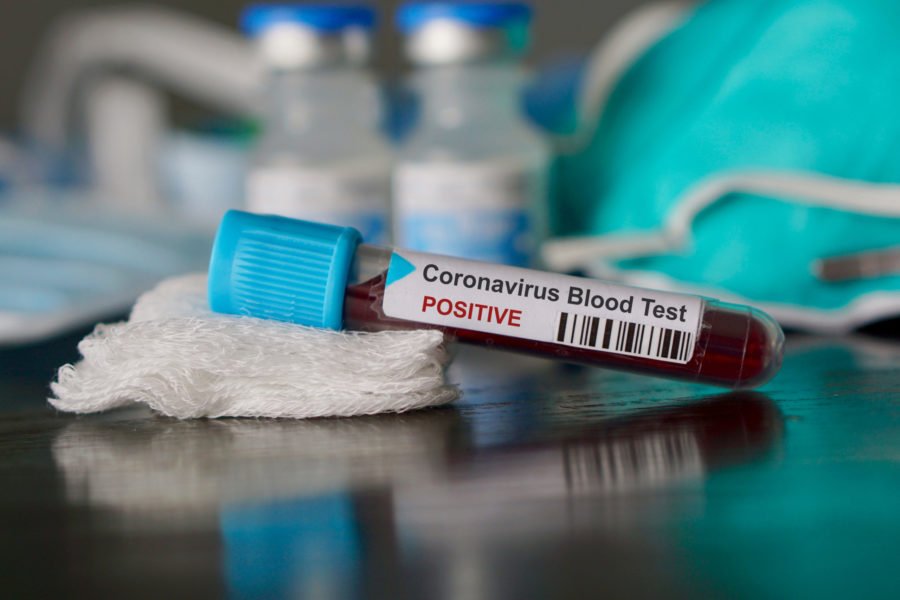
Σε ανακοίνωσή του σχετικά με την προμήθεια των τεστ ανίχνευσης του κοροναϊού ο ΕΟΦ ενημερώνει τους ενδιαφερόμενους ότι αυτά κατατάσσονται στα Ιατροτεχνολογικά προϊόντα. Συνεπώς, προϋπόθεση για την κυκλοφορία τους συνιστά η προηγούμενη κοινοποίηση στο Ηλεκτρονικό Μητρώο Ιατροτεχνολογικών προϊόντων ΕΟΦ (GREMDIS) όλων των στοιχείων που επιτρέπουν την αναγνώριση/ταυτοποίησή τους.
Ο Εθνικός Οργανισμός Φαρμάκων επισημαίνει ότι είναι αναγκαία η κοινοποίηση να γίνεται από τις On line Υπηρεσίες του ΕΟΦ.
Τα απαιτούμενα έγγραφα για την κοινοποίηση είναι:
- Βεβαίωση Αρμόδιας Αρχής του κράτους μέλους της Ε.Ε. όπου έγινε η εγγραφή των προϊόντων,2. Δήλωση Συμμόρφωσης του Κατασκευαστή (με αναφορά στον Εξουσιοδοτημένο Αντιπρόσωπό του για την Ε.Ε. όπου απαιτείται),3. Εξωτερική συσκευασία,
4. Οδηγίες Χρήσης.
Υπενθυμίζεται ότι στην περίπτωση κατασκευαστών σε Τρίτη χώρα, για να τεθούν τα προϊόντα τους στην αγορά της Ε.Ε., θα πρέπει να ορίζεται εξουσιοδοτημένο αντιπρόσωπο εγκατεστημένο στην Ε.Ε..Επομένως, η εταιρεία, η οποία διακινεί Ιατροτεχνολογικά προϊόντα πρέπει να φέρει βεβαίωση διακίνησης Ιατροτεχνολογικών Προϊόντων (Ι/Π) από Κοινοποιημένο Οργανισμό σύμφωνα με τα οριζόμενα στην Υπ. Απόφαση ΔΥ8δ/Γ.Π. οικ./1348/ΦΕΚ 32Β/16-1-2004 (Αρχές και κατευθυντήριες γραμμές ορθής πρακτικής διανομής Ι/Π).
Η εταιρεία διακίνησης θα πρέπει να μεριμνήσει πριν την κυκλοφορία των προϊόντων, η επισήμανση και οι οδηγίες χρήσης να είναι πλήρεις και ακριβείς στην Ελληνική γλώσσα, κατά την παράδοση στον τελικό χρήστη.
Από τον ΕΟΦ ανακοινώνονται ότι τα ενημερωτικά έγγραφα με στοιχεία για τα είδη των τεστ ανίχνευσής του κορωνοϊού και την πιστοποίησή τους από την Ευρωπαϊκή Επιτροπή και τον ECDC (European Centre for Disease Prevention and Control).
Τα έγγραφα είναι τα εξής:
1. An overview of the rapid test situation for COVID-19 diagnosis in the EU/EEA
2. Guidelines on COVID-19 in vitro diagnostic tests and their performance
https://ec.europa.eu/info/files/testing-kits-communication_en
3. Current performance of COVID-19 test methods and devices and proposed performance criteria
https://ec.europa.eu/docsroom/documents/40805
Διεύθυνση Αξιολόγησης Προϊόντων
Τμήμα Αξιολόγησης Υγειονομικού Υλικού


















Comments (0)