Το υπερβολικό σωματικό βάρος και η παχυσαρκία έχουν φτάσει σε ένα παγκόσμιο σημείο καμπής: το πρόβλημα αφορά περισσότερο από το 40% των ενηλίκων και το 20% των νέων και προβλέπεται να ξεπεράσει το 50% των ενηλίκων έως το 2030! Μετά από δεκαετίες στασιμότητας, μια νέα κατηγορία φαρμάκων, οι αγωνιστές GLP-1 (σεμαγλουτίδη, λιραγλουτίδη), έχουν μεταμορφώσει τη θεραπεία, αυξάνοντας τις προσδοκίες ασθενών και επενδυτών…
Παρακάτω, λοιπόν, θα δούμε πώς ακριβώς έχει η κατάσταση στην παγκόσμια αγορά, ποια είναι τα εμπόδια, ποιες νέες ουσίες βρίσκονται υπό ανάπτυξη και ποια φάρμακα είναι τα «φαβορί» για να τα βάλουν με το Ozempic και το Mounjaro.
Τα στοιχεία βασίζονται σε εκτιμήσεις της εταιρείας αναλύσεων της διεθνούς αγοράς Clarivate, που περιλαμβάνονται σε έκθεση με τίτλο “Drugs To Watch 2026”. Η έκθεση χαρτογραφεί ποιες φαρμακευτικές ουσίες –που έχουν εγκριθεί πρόσφατα ή βρίσκονται σε προχωρημένο στάδιο ανάπτυξης– είναι δυνατόν να εξελιχθούν σε blockbusters. Η παγκόσμια αγορά φαρμάκων για την παχυσαρκία μπορεί, λοιπόν, να φτάσει τα 150 δισ. δολ. έως το 2035 (Morgan Stanley, 2025), λόγω της ζήτησης για τα φάρμακα GLP-1 και τις μεταβολικές θεραπείες επόμενης γενιάς. Ωστόσο, οι διαπραγματεύσεις τιμολόγησης, οι συζητήσεις για την κάλυψη των πληρωτών, οι περιορισμοί στην προσφορά, τα πλαστά φάρμακα και οι επικείμενες λήξεις διπλωμάτων ευρεσιτεχνίας αποτελούν σημαντικά εμπόδια για την εμπορική πορεία των νέων θεραπειών.
Στις ΗΠΑ, οι συνταγογραφήσεις αγωνιστών GLP-1 για ενήλικες με υπερβολικό βάρος ή παχυσαρκία αυξήθηκαν κατά 586,7% από το 2019 έως το 2024. Καθώς τα φάρμακα αυτά επεκτείνονται και σε άλλες θεραπευτικές περιοχές, από την υγεία του εγκεφάλου έως τη νεφρική νόσο, ο ανταγωνισμός και η «όρεξη» για θεραπείες επόμενης γενιάς αυξάνονται.
Ο κατάλογος με τα υπό ανάπτυξη φάρμακα GLP-1 εξελίσσεται ραγδαία, με μεγάλες επενδύσεις που εκτείνονται σε διπλά και τριπλά ορμονικούς αγωνιστές (Πίνακας 1). Η χορήγηση από το στόμα και η μειωμένη συχνότητα δοσολογίας αποτελούν κρίσιμους διαφοροποιητικούς παράγοντες, που στοχεύουν στη βελτίωση της συμμόρφωσης και, ως εκ τούτου, των αποτελεσμάτων στον πραγματικό κόσμο.
ΠΙΝΑΚΑΣ 1
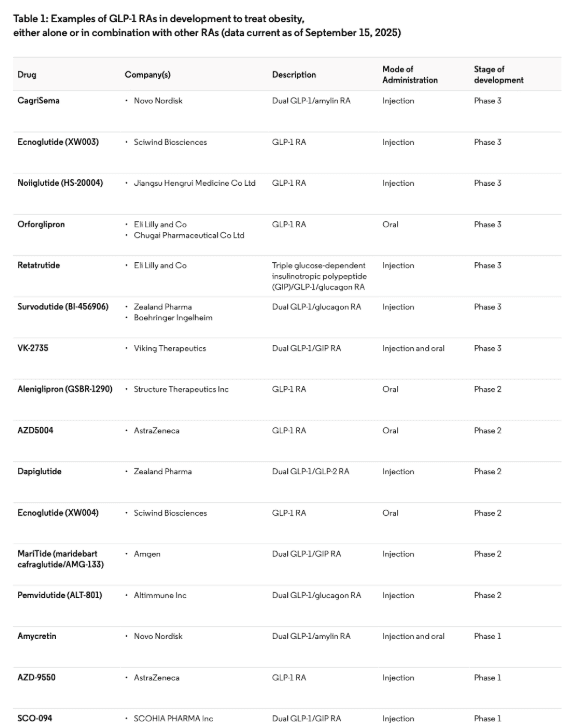
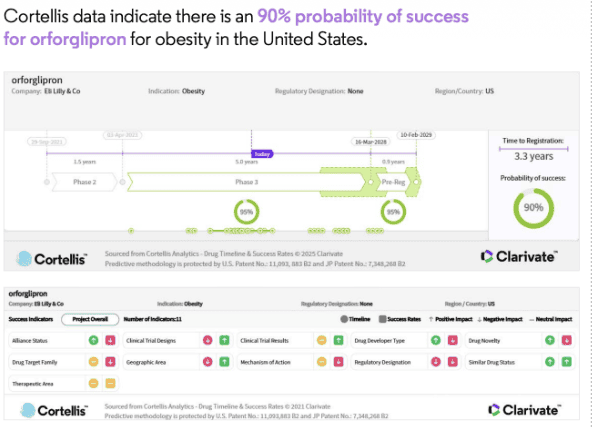
Για παράδειγμα, η ορφοργλιπρόνη (της Eli Lilly), ένας κορυφαίος υποψήφιος για θεραπεία με αγωνιστή GLP-1 από το στόμα, έδειξε πρόσφατα κλινικά σημαντική και στατιστικά σημαντική απώλεια βάρους, και συγκρίσιμες παρενέργειες με τα ενέσιμα στη μελέτη φάσης 2.
Τα από του στόματος GLP-1 θα μπορούσαν να βελτιώσουν τα μακροπρόθεσμα αποτελέσματα, ειδικά επειδή η χρήση των GLP-1 σε πραγματικές συνθήκες συχνά υπολείπεται της απώλειας βάρους, που παρατηρείται σε κλινικές δοκιμές, πιθανώς λόγω πρόωρης διακοπής ή χαμηλότερης δοσολογίας για την αντιμετώπιση δυσανεξιών. Και, δυστυχώς, η διακοπή συχνά οδηγεί σε σημαντική επαναπρόσληψη βάρους.
Σοβαρές παρενέργειες, όπως η παγκρεατίτιδα (Fair Health, 2025) και άλλες βλάβες οργάνων, έχουν επίσης σταματήσει ορισμένα αναπτυξιακά προγράμματα, όπως η απόφαση της Pfizer στα μέσα του 2025 να σταματήσει τον από του στόματος αγωνιστή υποδοχέα GLP-1 (δανουλιγιπρόνη) μετά από μία μόνο πιθανώς φαρμακευτική ηπατική βλάβη στη δοκιμή φάσης 3.
Η αμυλίνη (amylin) είναι μια ορμόνη που παράγεται από το πάγκρεας και παίζει καθοριστικό ρόλο στη ρύθμιση του σωματικού βάρους και του σακχάρου, γεγονός που την καθιστά έναν από τους πιο υποσχόμενους στόχους για την αντιμετώπιση της παχυσαρκίας, ενώ συχνά θεωρείται ο «διάδοχος» των GLP-1. Η αμυλίνη, λοιπόν, υπόσχεται μεγαλύτερη ανεκτικότητα από τους αγωνιστές GLP-1 και βρίσκεται στα σκαριά από πολλές εταιρείες:
- AstraZeneca: AZD6234 στη φάση 2
- Metsera Inc: MET-233i στη φάση 1
- Novo Nordisk: Amylin 355 και διπλός αγωνιστής αμυλίνης GLP-1/αμυλίνης αμυκρετίνη, και οι δύο στη φάση 1
- Structure Therapeutics: διπλός αγωνιστής αμυλίνης και καλσιτονίνης στο στάδιο που επιτρέπει την ανάπτυξη νέου φαρμάκου υπό έρευνα (IND).
Στοχεύοντας στην αμυλίνη ως την είσοδό της στην αγορά της παχυσαρκίας, η AbbVie σύναψε μια πιθανή συμφωνία ανάπτυξης και εμπορικής εκμετάλλευσης ύψους 1,875 δισ. δολ. στις αρχές του 2025 με την Gubra A/S, η οποία περιλάμβανε το Gubamy (GUB-014295), ένα ανάλογο αμυλίνης μακράς δράσης, που βρίσκεται επί του παρόντος σε φάση ανάπτυξης Ι. Η Gubra A/S επιδιώκει επίσης την ουροκορτίνη-2 ως στόχο για την παχυσαρκία, λόγω της πιθανής αποτελεσματικότητάς της στην απώλεια βάρους και του ευνοϊκού καρδιακού προφίλ. Ο υποδοχέας κανναβινοειδούς υποδοχέα 1 (CB1), ο οποίος συμβάλλει επίσης στην όρεξη, την αποθήκευση λίπους και τη ρύθμιση του μεταβολισμού, περιλαμβάνεται στον αναπτυσσόμενο κατάλογο της Novo Nordisk για την αντιμετώπιση της παχυσαρκίας.
Η ουσία Monlunabant (που αποκτήθηκε μέσω της εξαγοράς της Inversago Pharmaceuticals Inc, το 2023) επέδειξε στατιστικά σημαντική απώλεια βάρους, αν και με αναφορές για ήπιες έως μέτριες γαστρεντερικές και νευροψυχιατρικές παρενέργειες. Για την αποφυγή πιθανών νευροψυχιατρικών επιδράσεων, τόσο η Sky Bioscience Inc όσο και η Corbus Pharmaceuticals Holdings Inc στοχεύουν τον υποδοχέα CB1 με την ουσία nimacimab και την CRB-913, αντίστοιχα, ενώ ο στόχος της Monlunabant βρίσκεται στο κεντρικό νευρικό σύστημα (ΚΝΣ).
Άλλοι περιορισμοί των αγωνιστών GLP-1 που αντιμετωπίζονται περιλαμβάνουν την απώλεια μυϊκής μάζας, η οποία μπορεί να φτάσει έως και το 15%-40% του συνολικού χαμένου βάρους. Η ουσία Imagrumab (Eli Lilly), ένα μονοκλωνικό αντίσωμα που στοχεύει τόσο τους υποδοχείς ακτιβίνης IIA όσο και τους υποδοχείς IIB, στοχεύει στη διατήρηση της μυϊκής μάζας και στην προώθηση της μυϊκής ανάπτυξης. Σε μια δοκιμή φάσης 2b με σεμαγλουτίδη, το 92,8% της απώλειας βάρους προήλθε από τη λιπώδη μάζα έναντι 71,8% με τη σεμαγλουτίδη μόνο (American Diabetes Association, 2025).
Αρχικά, ανακαλύφθηκε από τη MorphoSys και αναπτύχθηκε από τη Novartis για μυοσίτιδα, μια σπάνια αυτοάνοση διαταραχή μυϊκής απώλειας, η ουσία bimagrumab, όμως απέτυχε στη δοκιμή φάσης 2/3 και παραχωρήθηκε με άδεια στη Versanis Bio για τη διαχείριση βάρους. Η Eli Lilly απέκτησε τη Versanis και τη bimagrumab σε μια συμφωνία αξίας έως και 1,9 δισ. δολ. τον Αύγουστο του 2023.
Ορφοργλιπρόνη
Η ορφοργλιπρόνη είναι ο πρώτος από του στόματος αγωνιστής GLP-1 που φτάνει σε δοκιμές φάσης 3. Μπορεί να ληφθεί χωρίς περιορισμούς τροφής ή νερού, οποιαδήποτε στιγμή της ημέρας. Ως εκ τούτου, αντιπροσωπεύει μια σημαντική ανακάλυψη στην ευκολία και την προσβασιμότητα σε σύγκριση με τις ενέσιμες εναλλακτικές λύσεις. Είναι επίσης πιο βολική από την από του στόματος σεμαγλουτίδη (RYBELSUS της Novo Nordisk), η οποία έχει αυστηρές απαιτήσεις δοσολογίας, που οι ασθενείς συχνά δυσκολεύονται να τηρήσουν.
Η ορφοργλιπρόνη είναι επίσης ευκολότερη και λιγότερο ακριβή στην παραγωγή από τους αγωνιστές GLP-1 που βασίζονται σε πεπτίδια και δεν απαιτεί απαιτήσεις ψυχρής αποθήκευσης, κάτι που θα μπορούσε να βελτιώσει τη διαθεσιμότητα θεραπείας με GLP-1 παγκοσμίως. Επιπλέον, η Eli Lilly έχει ήδη «φυλάξει» 548 εκατ. δολ., υποδηλώνοντας εμπιστοσύνη στην κυκλοφορία πλήρους κλίμακας χωρίς περιορισμούς.
Τα κορυφαία αποτελέσματα από τις παγκόσμιες δοκιμές φάσης 3, μέχρι σήμερα, καταδεικνύουν ότι η ορφοργλιπρόνη προσφέρει παρόμοια ή ανώτερη αποτελεσματικότητα από τα περισσότερα διαθέσιμα προϊόντα GLP-1, συμπεριλαμβανομένης της από του στόματος σεμαγλουτίδης, διατηρώντας παράλληλα ένα προφίλ ασφάλειας και ανεκτικότητας συμβατό με την καθιερωμένη κατηγορία ενέσιμων GLP-1. Τα δεδομένα από τις δοκιμές φάσης 3 ATTAIN-1 και ATTAIN-2 για την παχυσαρκία αναμένεται να υποστηρίξουν τις πρώτες κανονιστικές υποβολές για την παχυσαρκία στα τέλη του 2025/αρχές 2026.
Παρ’ όλο που το ποσοστό απώλειας βάρους 12,4% στη δοκιμή ATTAIN-1 ήταν μικρότερο από το αναμενόμενο (περίπου 16%), τα αποτελέσματα εξακολουθούν να υποστηρίζουν την κανονιστική έγκριση. Η Eli Lilly σχεδιάζει να υποβάλει δεδομένα για την ορφοργλιπρόνη σε ρυθμιστικές αρχές για τον Σακχαρώδη Διαβήτη τύπου 2 το πρώτο εξάμηνο του 2026.
Ρετατρουτίδη
Η ρετατρουτίδη, η οποία αναμένεται να είναι ο πρώτος τριπλός αγωνιστής στην κατηγορία του που στοχεύει τους υποδοχείς γλυκαγόνης GIP και GLP-1, είναι ένα μόνο πεπτίδιο που έχει σχεδιαστεί για να ρυθμίζει πολλαπλές μεταβολικές οδούς που είναι κρίσιμες για την ενεργειακή ομοιόσταση του σώματος.
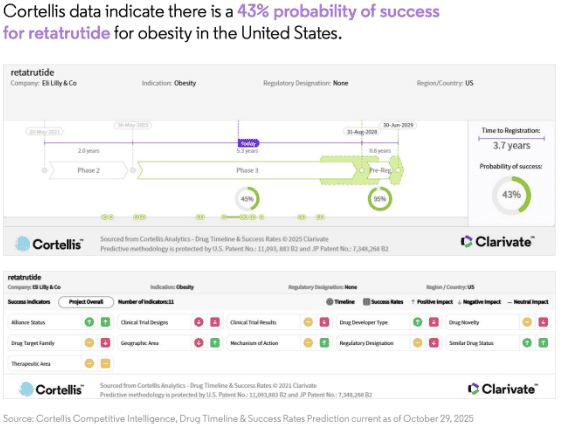
Ως αποτέλεσμα, θα μπορούσε να επιτρέψει πρωτοφανείς μεταβολικές επιδράσεις σε σχέση με τις τρέχουσες θεραπείες που στοχεύουν μόνο έναν ή δύο υποδοχείς, με αποτέλεσμα ενδεχομένως μεγαλύτερη απώλεια βάρους από το Zepbound/Mounjaro, όχι μόνο μειώνοντας την πρόσληψη θερμίδων, αλλά και αυξάνοντας την ενεργειακή κατανάλωση μέσω της διέγερσης των υποδοχέων γλυκαγόνης.
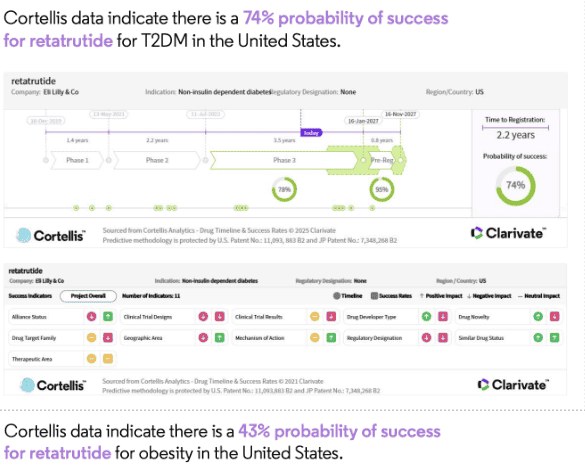
Στη μελέτη φάσης 2 για την παχυσαρκία, η ρετατρουτίδη ήταν το πρώτο φάρμακο που πέτυχε τουλάχιστον 5% απώλεια βάρους σε όλους τους συμμετέχοντες. Τα αποτελέσματα περιγράφηκαν ως επίτευξη απώλειας βάρους «χειρουργικού επιπέδου» (μέσος όρος 24,2%) στις 48 εβδομάδες και περίπου το 25% των ασθενών στην υψηλότερη δόση πέτυχαν απώλεια βάρους ≥30%.
Η ρετατρουτίδη ήταν ασφαλής και η ανεκτικότητα ήταν σύμφωνη με τη φαρμακολογία των αγωνιστών GLP-1. Σε μια υπομελέτη που διεξήχθη με ασθενείς με παχυσαρκία και NASH (μη αλκοολική στεατοηπατίτιδα), η ρετατρουτίδη μείωσε το ηπατικό λίπος έως και 82%, και το 86% των ασθενών πέτυχε φυσιολογικά επίπεδα ηπατικού λίπους (≤5%). Η μελέτη άμεσης σύγκρισης της ρετατρουτίδης έναντι του Ozempic (σεμαγλουτίδη, Novo Nordisk) στον ΣΔ τύπου 2 είναι επίσης αξιοσημείωτη, επειδή η υποδόρια σεμαγλουτίδη είναι ένας από τους πιο αποτελεσματικούς παράγοντες GLP-1 όσον αφορά τη μείωση της HbA1c και την απώλεια βάρους. Επομένως, η αποδεδειγμένη ανωτερότητα ή ακόμη και η μη κατωτερότητα στη μελέτη θα μπορούσε να προσφέρει στη ρετατρουτίδη ένα σημαντικό πλεονέκτημα στην αγορά, έναντι των υπαρχουσών θεραπειών. 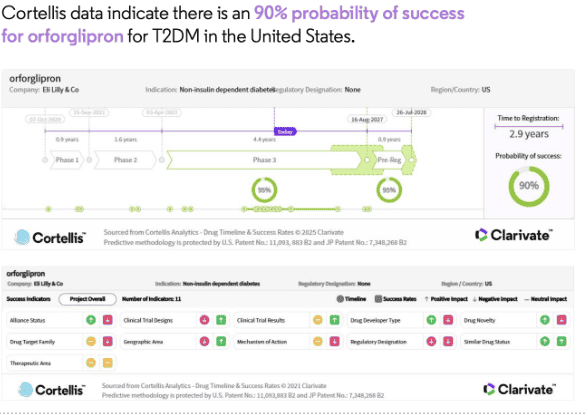
Βρίσκονται σε εξέλιξη βασικές δοκιμές φάσης 3 για την επιβεβαίωση και επέκταση των αποτελεσμάτων φάσης 2, με τα κορυφαία αποτελέσματα από τη δοκιμή TRIUMPH-4 φάσης 3 να καταδεικνύουν σημαντική απώλεια βάρους και βελτιώσεις στον πόνο και τη σωματική λειτουργία σε άτομα με παχυσαρκία και οστεοαρθρίτιδα γόνατος.
Πώς θα επηρεάσουν η ορφοργλιπρόνη και η ρετατρουτίδη την αγορά για την παχυσαρκία και τον ΣΔ τύπου 2;
Οι κύριες ουσίες φάσης 3 για την παχυσαρκία, συμπεριλαμβανομένων των CagriSema, ορφοργλιπρόνης, ρετατρουτίδης και survodutide (Boehringer Ingelheim), ξεπερνούν την απώλεια βάρους, με ιδιαίτερη έμφαση στη θεραπεία συννοσηροτήτων, όπως οι καρδιαγγειακές παθήσεις, η αποφρακτική άπνοια ύπνου, η οστεοαρθρίτιδα, η χρόνια νεφρική νόσος (CKD) και η MASH, οι οποίες θα μπορούσαν επίσης να βελτιώσουν τη χρήση τους στην παχυσαρκία και τον ΣΔ τύπου 2.
Από αυτές η survodutide είναι ένας διπλός παράγοντας GLP-1/γλυκαγόνης, που πιθανότατα θα κυκλοφορήσει στις ΗΠΑ έναν χρόνο νωρίτερα από τη ρετατρουτίδη, γεγονός που την καθιστά το πρώτο φάρμακο για την παχυσαρκία που χρησιμοποιεί γλυκαγόνη ως νέο μηχανισμό δράσης.
Η ορφοργλιπρόνη και η ρετατρουτίδη είναι έτοιμες να επεκτείνουν τους ασθενείς που θα ξεκινήσουν θεραπεία με παράγοντα GLP-1. Τα αποτελέσματα από συνεχιζόμενες συγκριτικές δοκιμές, όπως οι ACHIEVE-2, ACHIEVE-3 και TRIUMPH-5, θα είναι κρίσιμα για τον προσδιορισμό της θέσης αυτών των θεραπειών στην αγορά της παχυσαρκίας και του σακχαρώδη διαβήτη τύπου 2.
Ορφοργλιπρόνη
Η χρήση της ορφοργλιπρόνης αναμένεται να προτιμηθεί από γιατρούς και ασθενείς λόγω του ότι χορηγείται από το στόμα, αλλά και γιατί έχει ευελιξία στη λήψη, ενώ η συνολική αποτελεσματικότητά της φαίνεται να μην υπολείπεται των ενέσιμων θεραπειών που είναι σήμερα διαθέσιμες.
Η ορφοργλιπρόνη έχει επιδείξει σημαντική μείωση της HbA1c και απώλεια βάρους στο πρόγραμμα ACHIEVE για τον ΣΔ2, για αυτό και αποτελεί μια ισχυρή εναλλακτική λύση για ασθενείς που αναζητούν μη ενέσιμες επιλογές. Η βελτιωμένη βιοδιαθεσιμότητά της και η απλοποιημένη δοσολογία της αναμένεται να ενισχύσουν την ελκυστικότητά της σε σύγκριση με το RYBELSUS. Επιπλέον, η βολική από του στόματος σύνθεσή της είναι πιθανό να υποστηρίξει την προηγούμενη χρήση στον αλγόριθμο θεραπείας, ανταγωνιζόμενη άλλα από του στόματος αντιδιαβητικά φάρμακα, όπως οι αναστολείς DPP-4.
Τόσο στις δοκιμές ACHIEVE-2 όσο και στις δοκιμές ACHIEVE-3, όλες οι δόσεις της ορφοργλιπρόνης ξεπέρασαν τις ουσίες με τις οποίες έγινε σύγκριση (FARXIGA και RYBELSUS, αντίστοιχα) στη μείωση της HbA1c σε άτομα με ΣΔ2. Το συνολικό προφίλ ασφάλειας και ανεκτικότητας της ορφοργλιπρόνης ήταν σύμφωνο με προηγούμενες μελέτες, και οι πιο συχνές ανεπιθύμητες ενέργειες ήταν ήπιες έως μέτριες γαστρεντερικές παρενέργειες. Τα θετικά αποτελέσματα από τη δοκιμή ATTAIN-MAINTAIN πιθανότατα θα δημιουργήσουν μια ευκαιρία στην αγορά για την ορφοργλιπρόνη ως ένα ελκυστικό φάρμακο διατήρησης βάρους μετά τη διακοπή των πιο αποτελεσματικών φαρμάκων κατά της παχυσαρκίας.
Η ορφοργλιπρόνη προβλέπεται να κατακτήσει περίπου το 3% έως 12% του μεριδίου των ασθενών στους πληθυσμούς ΣΔ τύπου 2 και παχυσαρκίας, αντίστοιχα, στις αγορές της G7 έως το 2033. Ωστόσο, τα από του στόματος χορηγούμενα προϊόντα GLP-1, συμπεριλαμβανομένης της ορφοργλιπρόνης, δεν αναμένεται να ξεπεράσουν τα υποδορίως χορηγούμενα σκευάσματα GLP-1 έως το 2033.
Ρετατρουτίδη
Από την άλλη πλευρά, η ρετατρουτίδη αναπτύσσεται με μεγαλύτερη έμφαση στην παχυσαρκία. Εάν η ρετατρουτίδη επιδείξει μη κατωτερότητα ή ανωτερότητα στα γλυκαιμικά αποτελέσματα και τα αποτελέσματα βάρους, θα μπορούσε να αναδειχθεί ως ισχυρός ανταγωνιστής των καθιερωμένων ενέσιμων θεραπειών GLP-1, όπως οι Mounjaro/Zepbound.
Το αναμενόμενο ανώτερο προφίλ αποτελεσματικότητας της ρετατρουτίδης την τοποθετεί σε θέση να κατακτήσει σημαντικό μερίδιο αγοράς από τις υπάρχουσες θεραπείες GLP-1, αν και, δεδομένου του μηχανισμού δράσης της, της οδού χορήγησης και του αναμενόμενου υψηλού κόστους, η ρετατρουτίδη πιθανότατα θα συνταγογραφείται μετά από σταδιακή θεραπεία, παρόμοια με τις τρέχουσες πρακτικές συνταγογράφησης των υποδόριων GLP-1 για τον ΣΔ2.
Αν και η έλλειψη εξοικείωσης με τα ανάλογα γλυκαγόνης θα μπορούσε να συμβάλει σε μια σχετικά αργή υιοθέτηση μετά την κυκλοφορία για την παχυσαρκία, η ρετατρουτίδη έχει υψηλό δυναμικό χρήσης, που οφείλεται στην ικανότητά της να επιφέρει μεγαλύτερη απώλεια βάρους από τις υπάρχουσες θεραπείες και στα ευνοϊκά δεδομένα σύγκρισης έναντι της τιρζεπατίδης.
Μετά το 2028, η ρετατρουτίδη αναμένεται να γίνει ο κύριος μοχλός ανάπτυξης για την αγορά φαρμάκων για την παχυσαρκία, με τη δυναμική να αντικατοπτρίζει τη μετάβαση της Novo Nordisk από το Wegovy στο CagriSema, μεταφέροντας τους ασθενείς σε ένα μόριο επόμενης γενιάς προτού η τιρζεπατίδη χάσει την προστασία ευρεσιτεχνίας της στα μέσα του 2030.
Ποια κενά στη θεραπεία καλύπτουν αυτές οι θεραπείες
Παρ’ όλο που η πλειονότητα των φαρμάκων GLP-1 είναι ενέσιμα, οι γιατροί γενικά δεν θεωρούν την οδό χορήγησης σημαντικό εμπόδιο. Παρ’ όλα αυτά, παρά τη μετασχηματιστική τους επίδραση στη διαχείριση του βάρους και του ΣΔ2, τα ποσοστά διακοπής της θεραπείας με φάρμακα GLP-1 είναι υψηλά, λόγω της υψηλής τιμής τους, των προβλημάτων ανεκτικότητας και της μη βέλτιστης (ή ανεπαρκούς) αποτελεσματικότητάς τους, οδηγώντας σε επαναπρόσληψη βάρους και κακό γλυκαιμικό έλεγχο. Επιπλέον, τα φάρμακα GLP-1 και GLP-1/GIP παραμένουν ακριβά σε αγορές όπως οι Ηνωμένες Πολιτείες και συνεχίζουν να έχουν περιορισμένη κάλυψη από τους φορείς πληρωμής.
Με την κυκλοφορία πιο βολικών φαρμάκων, όπως η από του στόματος χορήγηση ορφοργλιπρόνης χωρίς περιορισμούς νηστείας, και τα διπλά και τριπλά φάρμακα GLP-1, που θα μπορούσαν να είναι πιο αποτελεσματικά για την παχυσαρκία και τον ΣΔ2, τα εμπόδια στη συμμόρφωση και την κάλυψη θα μπορούσαν να βελτιωθούν, και να γίνουν αυτά τα φάρμακα διαθέσιμα σε μεγαλύτερο πληθυσμό.
Ποια εμπόδια μπορεί να χρειαστεί να ξεπεράσουν για να φτάσουν σε επίπεδο επιτυχίας
Τα αποτελέσματα της δοκιμής ACHIEVE-3 έναντι του ενέσιμου RYBELSUS είναι πιθανό να είναι καθοριστικά για την πορεία της ορφοργλιπρόνης. Ομοίως, θα πρέπει να επιδείξει κλινικά σημαντικές μειώσεις της HbA1c, απώλεια βάρους και οφέλη στα αποτελέσματα για να ανταγωνιστεί τις διαθέσιμες αντιδιαβητικές θεραπείες. Διαφορετικά, μπορεί να δυσκολευτεί να κερδίσει την εμπιστοσύνη των γιατρών και να διαφοροποιηθεί από τις εδραιωμένες θεραπευτικές επιλογές.
Η ρετατρουτίδη όχι μόνο θα εισέλθει στην αγορά αργότερα από τους ανταγωνιστές της, αλλά θα αντιμετωπίσει επίσης άμεσο ανταγωνισμό από τα γενόσημα CagriSema, Wegovy και σεμαγλουτίδης, κάτι που θα μπορούσε να αποτελέσει εμπόδιο μετά την κυκλοφορία του.
Ακόμη, η καρδιαγγειακή ασφάλεια αποτελεί σημαντική παράμετρο για τις ρυθμιστικές αρχές και τους γιατρούς, επομένως η επίδειξη θετικών καρδιαγγειακών αποτελεσμάτων θα συνεχίσει να αποτελεί απαίτηση μετά την κυκλοφορία του προϊόντος στην αγορά και να είναι κρίσιμη για την έγκριση των γιατρών και των φαρμακοποιών τόσο για την παχυσαρκία όσο και για τον ΣΔ2.





















Comments (0)